Vitor Souza Magalhães; Milena Souza Ribeiro Santos; Marina Viegas Moura Rezende Ribeiro
DOI: 10.17545/eOftalmo/2024.0013
RESUMO
OBJETIVOS: A doença do olho seco é definida como uma doença multifatorial das lágrimas e da superfície ocular que desencadeia sintomas de desconforto, instabilidade visual e alteração lacrimal. Apesar da maximização das terapêuticas convencionais, alguns pacientes são refratários, persistindo com sinais e sintomas, se beneficiando de terapias adicionais, como os hemocomponentes e hemoderivados. O objetivo foi realizar uma revisão integrativa da literatura indexada nos últimos 10 anos, verificar e examinar o conhecimento descrito sobre o tratamento da doença do olho seco utilizando hemocomponentes e hemoderivados.
MÉTODO: O estudo foi definido como uma revisão integrativa, sendo feito buscas nas fontes de dados MEDLINE, LILACS, SciELO e EMBASE, utilizando os descritores: "síndrome do olho seco", "doença do olho seco", "tratamento do olho seco", "sangue", "soro" e "plasma rico em plaquetas". Foram identificados 597 publicações potencialmente elegíveis, selecionando-se, ao final, 16 ensaios clínicos randomizados e não randomizados que atendiam aos critérios de inclusão.
RESULTADOS: A maioria dos estudos analisados (9) abordou o tratamento com soro autólogo, sete estudos avaliaram com concentrado de plaquetas.
CONCLUSÃO: A terapêutica com hemocomponentes e hemoderivados mostrou ser segura e efetiva, sendo uma opção válida para os pacientes refratários às terapias tradicionais. Ressalta-se a importância da realização de novos estudos clínicos, com maior amostra, para melhor estabelecimento e padronização dos processos e formulações a serem utilizadas no tratamento da doença do olho seco.
Palavras-chave: Síndrome do olho seco; Doença do olho seco; Tratamento do olho seco; Sangue; Soro; Plasma rico em plaquetas.
ABSTRACT
PURPOSES: Dry eye syndrome is defined as a multifactorial disease of the tears and the ocular surface, which triggers symptoms such as visual discomfort, visual instability, and lacrimal defects. Despite the optimization of conventional therapies, some patients are refractory, persisting with signs and symptoms. However, such patients can benefit from additional therapies that use blood components and blood derivatives. This study aimed to conduct an integrative review of the indexed literature over the last decade to verify and examine the knowledge available regarding the treatment of dry eye disease using blood components and blood products.
METHODS: The study was an integrative review, and searches were performed on MEDLINE, LILACS, SciELO, and EMBASE databases using the search terms: "dry eye syndrome," "dry eye disease," "dry eye treatment," "blood," "serum," and "platelet-rich plasma" as well as their equivalent terms in Portuguese. Overall, 597 potentially eligible publications were identified, and 16 randomized and non-randomized clinical trials that met the inclusion criteria were selected.
RESULTS: Most of the studies analyzed (9) included treatment with autologous serum, and seven studies evaluated platelet concentrates.
CONCLUSION: Therapy with blood components and blood derivatives has been proven to be safe and effective; moreover, it is a valid option for patients who are refractory to traditional therapies. It is crucial to perform further clinical studies with a larger sample size to better establish and standardize the processes and formulations that can be used in the treatment of dry eye syndrome.
Keywords: Dry eye syndrome; Dry eye disease; Dry eye treatment; Blood; Serum; Platelet-rich plasma.
INTRODUÇÃO
A doença do olho seco (DOS) acomete de 5% a 34% da população mundial1 sendo definida pelo Dry Eye Workshop (DEWS II) como uma doença multifatorial das lágrimas e da superfície ocular que desencadeia sintomas de desconforto, instabilidade visual e alteração lacrimal com possibilidade de dano óptico em consequência do aumento da osmolaridade do filme lacrimal e inflamação ocular2. Sabe-se que muito se avançou ao longo dos últimos anos no campo de estudo da sua fisiopatologia e tratamento. No entanto, torna-se necessário o constante estudo terapêutico da doença devido à sua cronicidade e busca por um tratamento etiológico específico3.
As lágrimas desempenham um papel essencial na saúde da superfície ocular pois seus componentes são atuantes na regulação, proliferação, diferenciação e maturação do epitélio4. O tratamento convencional para DOS inclui lágrimas artificiais (LA), corticosteroides tópicos, Ciclosporina-A, lentes de contato terapêuticas, e oclusão do ponto lacrimal5. As LA, apesar de amplamente disponíveis, carecem das propriedades biológicas que promovem a renovação da superfície ocular e a defesa imunológica6. Apesar da maximização dessas terapêuticas, alguns pacientes são refratários, persistindo com sinais e sintomas da DOS severa e se beneficiam de terapias adicionais como o uso de hemocomponentes e hemoderivados a partir do processamento do sangue do doador7.
O soro autólogo (SA), foi utilizado pela primeira vez em 1984 por Fox et al. no tratamento da DOS em pacientes refratários ao uso de lágrimas artificiais8. O SA possui sua osmolaridade e propriedade biomecânicas similares às lágrimas naturais, além de ser livre de conservantes, o que reduz a incidência de alergia e toxicidade9. Desde então o SA tem sido usado com sucesso no tratamento da DOS severa relacionada a diversas condições, como a síndrome de Sjögren (SS), ceratite límbica superior, síndrome de Stevens-Johnson entre outras10. A SS é uma doença sistêmica autoimune caracterizada por inflamação crônica que resulta em xerostomia e DOS, ela se divide em primária (ausência de outra doença do tecido conjuntivo) e secundária (associada a outras doenças sistêmicas, como lúpus, artrite reumatoide e escleroderma)11. Os efeitos terapêuticos SA decorrem pelo fato do seu pH e osmolaridade serem similares ao filme lacrimal. Seu mecanismo de ação baseia-se em propriedades lubrificantes e a concentração de vitaminas A e E, fatores de crescimento, fibronectina e citocinas capazes de promover o trofismo celular dentro do epitélio, melhorando sua regeneração12. Além disso, o SA propõe melhora epitelial através da ligação e neutralização por citocinas inflamatórias. O SA contém componentes bactericidas lisozima, lactoferrina e imunoglobulinas, reduzindo assim o risco de contaminação e infecção de pacientes acometidos pelo olho seco3.
O uso de concentrado de plaquetas (CP) tem efeito antiapoptótico nas células do estroma da córnea e tornou-se uma estratégia válida no manejo de diversos distúrbios da superfície ocular, incluindo úlceras de córnea e defeitos epiteliais persistentes, secundários à DOS moderada e severa13. Recentemente o uso do CP, tem se destacado, por ter vantagens frente ao SA, como a maior quantidade de fatores de crescimento epitelial e vitamina A e ser livre de citocinas inflamatórias14.
As complicações com uso de hemocomponentes e hemoderivados no tratamento da DOS são raras, sobretudo quando seguidos os protocolos de segurança na preparação e armazenamento, e quando existem são bem toleradas. Os pacientes podem desenvolver desconforto ocular, ligeira epiteliopatia, conjuntivite bacteriana ou eczema palpebral15. A terapia pode ser contraindicada a alguns grupos: crianças, idosos, pacientes com infecção bacteriana sistêmica severa, doença autoimune aguda ou aqueles com medo de flebotomia. Também pode ser contraindicada para pacientes com restrições à doação de sangue autólogo: insuficiência cardíaca congestiva, estenose aórtica grave, ataque cardíaco ou acidente vascular cerebral nos últimos 6 meses, angina, doença cianótica, infecção ou uso de antibióticos16.
MÉTODOS
Foi realizada uma revisão integrativa da literatura por meio de pesquisa e avaliação criteriosa dos estudos publicados sobre a temática proposta. Esse método de pesquisa objetiva traçar uma análise sobre o conhecimento já construído em pesquisas anteriores sobre um determinado tema17.
A coleta de dados foi realizada entre os meses de maio a outubro de 2022, sendo a estratégia de busca realizada nos idiomas português e inglês, com o objetivo de responder a seguinte pergunta: "Quais são os tratamentos com hemocomponentes e hemoderivados disponíveis para a doença do olho seco?". Desse modo, foi realizada busca por ensaios clínicos randomizados e não randomizados publicados no período entre 2012 e 2022, nas bases de dados MEDLINE, LILACS, SciELO e EMBASE. A estratégia de busca utilizada utilizou os descritores síndrome do olho seco; doença do olho seco OR tratamento do olho seco) AND (sangue OR soro OR plasma rico em plaquetas)) e seus respectivos em inglês ((dry eye syndrome OR dry eye disease OR dry eye treatment) AND (blood OR serum OR platelet-rich plasma)) construída a partir de descritores disponíveis na terminologia Descritores em Ciências da Saúde (DECS), articulados pelos operadores booleanos OR e AND.
Após busca nas bases supracitadas, os seguintes critérios de inclusão foram adotados: ensaios clínicos randomizados e não-randomizados publicados em Português e Inglês; relacionados ao tratamento do olho seco com hemocomponentes ou hemoderivados; ensaios com humanos; publicados entre 2012 e 2022; disponibilidade de texto completo em suporte eletrônico; publicado em periódicos nacionais e internacionais. Critérios de exclusão: tratamento com hemocomponentes ou hemoderivados não relacionado a DOS; publicação sem relação significativa com as palavras-chave; publicação em línguas não cobertas no critério de inclusão.
O fluxograma (Figura 1) demonstra como os artigos foram escolhidos, começando com uma seleção apenas do título de trabalhos que não incluíam artigos de revisão, relatos de caso, relatos de experiência e outras pesquisas não quantitativas que não poderiam ser incluídas em uma revisão integrativa. Após essa triagem inicial, os trabalhos que responderam à questão norteadora e se enquadram na descrição da pesquisa, foram escolhidos por meio da leitura do resumo 60 artigos e 16 foram finalmente escolhidos após a leitura na íntegra. Além disso, foram pesquisadas listas de citações e referências bibliográficas pertinentes ao objetivo do estudo.
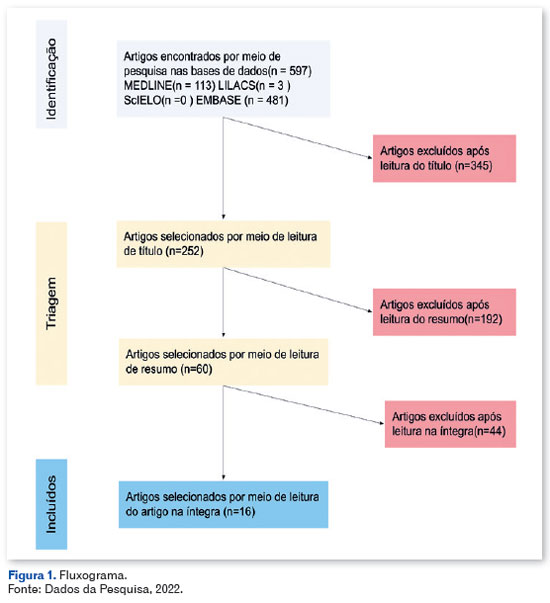
RESULTADOS
O período de coleta de dados ocorreu durante o primeiro e segundo semestres de 2022. Os artigos selecionados foram lidos e as informações extraídas e organizadas mediante as variáveis: autor/ano, tipo de estudo, local de publicação, terapia e resultados, dispostas na tabela 1.
Dezessete pacientes adultos portadores de DOS severa bilateral fizeram parte de um ensaio clínico, durante 3 meses, utilizando CSA a 20% no máximo 12 vezes ao dia, 15 minutos após aplicação de LA. Houve melhora significativa no exame clínico através do BUT (1,7s para 2,2s) e também do TS (1.1mm para 2.2mm). Em relação aos sintomas subjetivos, houve melhora gradual, estatisticamente significativa, na sensação de secura, desconforto, sensação de corpo estranho e fotofobia. A avaliação clínica foi feita antes da terapia e ao final dos 3 meses, houve melhora significativa em 72% dos pacientes examinados, em uso do CSA, sobretudo da sensação de corpo estranho18.
Cho et al., comparou a eficácia de CSA a 100% com 3 diluições de CSA diferentes(50% + SF0.9%, 50% + LA, 50% + Ceftazidima) no tratamento de 85 pacientes divididos em 3 grupos, Grupo I - Portadores SS, Grupo II - Não portadores de SS e Grupo III - Defeitos epiteliais persistentes. Todos os grupos foram submetidos à avaliação da velocidade de reparo epitelial, utilizando a medição da área (mm2/dia) na lâmpada de fenda. Nos portadores de SS, o CSA não diluído obteve uma velocidade de reparo significativamente maior quando comparado às outras 3 diluições de CSA a 50%12.
O ensaio clínico randomizado conduzido por Celebi et al., avaliou a eficácia do CSA a 20% em comparação com LA sem conservantes, em pacientes portadores de DOS severa. Esse estudo incluiu 20 pacientes(18 mulheres e 2 homens) refratários ao tratamento convencional onde observou-se melhora significativa dos sintomas, sem efeitos adversos, após 1 mês de uso do CSA, em comparação com o grupo LA. Essa melhora foi evidenciada através da análise quantitativa do teste de Schirmer (TS), teste de ruptura do filme (TRF) e questionário OSDI (Ocular Surface Disease Index-Allergan)4.
Hwang et al. avaliaram os efeitos, em 20 pacientes portadores de SS primária e 14 portadores de SS secundária, durante 4 semanas de terapia com CSA a 50%. Houve melhora significativa dos sintomas na SS primária, o que não foi evidenciado na SS secundária. A análise da concentração das seguintes citocinas pró inflamatórias TNF-a, IL-1b, IL-6, e IL-8, resultou em valores mais elevados na SS secundária. Por esse motivo, foi sugerido pelos autores, que o CSA não é eficaz no tratamento da DOS em portadores de SS secundária11.
O estudo conduzido por Yilmaz et al., comparou a efetividade do CSA a 40% com a LA no tratamento de pacientes com DOS, secundária ao uso de ácido retinóico sistêmico (isotretinoína). Pacientes com outras patologias prévias da superfície ocular foram excluídos. A isotretinoína reduz a função da glândula meibomiana, produtora do componente lipídico da lágrima, levando a DOS. Nesse ensaio clínico randomizado, o CSA a 40% se mostrou uma alternativa efetiva comparada às LA sem conservantes1.
Alguns pacientes possuem limitação logística (deslocamento do paciente até o centro de coleta e tempo de processamento da amostra) ou incapacidade clínica(dificuldade no acesso venoso, baixos níveis de hemoglobina, medo de agulhas e idade do paciente) de utilizar o seu próprio sangue na preparação do CSA. Com isso em mente, van der Meer et al. , realizaram um ensaio clínico randomizado com 15 pacientes portadores de DOS grave, onde foi comparado a eficácia e tolerabilidade do uso do colírio produzido a partir do soro autólogo e soro alogênico (originado de outros doadores), porém, não foi encontrado diferença significativa, tendo eficácia e tolerabilidade comparáveis19.
Ribeiro et al. avaliou a eficácia do CCP autólogo, aplicado quatro vezes ao dia, durante um mês no olho seco sintomático de 12 pacientes diabéticos refratários a terapias convencionais. Todos os pacientes apresentaram melhora de sintomas e sinais nos testes adotados: TS e TRF16. Após 6 meses, Ribeiro et al., avaliaram, de forma inédita, a persistência dos efeitos da terapia com CCP. Os pacientes passaram 5 meses em uso de LA de sua preferência, após a terapia inicial de 1 mês com CCP. Os escores do OSDI e TRF mostraram valores superiores aos basais de 6 meses antes da terapia, o que corrobora com a tese de efeito prolongado14.
No ensaio clínico randomizado, conduzido por Garcia-Conca et al., 84 pacientes com olho seco hipossecretor, divididos em dois grupos, da seguinte forma: 44 tratados com CCP e 39 com LA. As alterações nos TS e TRF foram avaliadas durante 30 dias do tratamento. O grupo tratado com CCP apresentou superioridade nos seguintes aspectos quando comparados ao grupo em uso de LA: redução dos sintomas, melhora visual, redução da hiperemia e melhora no TS20.
O uso de CCP a 20% em comparação com o CSA a 20%, 10 gotas em cada olho durante 1 mês, em grupo de 10 pacientes de um ensaio clínico randomizado, realizado por Metheetrairut et al.,evidenciou melhora significativa no TS e teste de acuidade visual para o CCP a 20%. Nenhum efeito adverso foi relatado pelas pacientes do estudo21.
A terapia de ICP na GL mostrou-se superior a LA no tratamento da disfunção glandular, em ensaio clínico randomizado com 13 pacientes diagnosticados com SS, no qual foram aplicadas ICP, de forma espaçada, nos dias 0, 30, 60 e 90. O volume lacrimal aumentou significativamente quando comparado com o grupo em uso de LA13.
O estudo conduzido por Allam, randomizou 20 pacientes, 40 olhos, em dois grupos, o primeiro recebeu ICP na GL, de forma espaçada, nos dias 0,30,60 e 90. O segundo grupo recebeu CSA a 50% cinco vezes ao dia. Ao fim das doze semanas de estudo, ambas terapias se mostraram comparáveis em termos de efetividade. Embora a ICP seja uma terapia dolorosa, foi contornado com a injeção anestésica, na região da GL, 5 minutos antes da aplicação. Apesar de nenhuma complicação ter sido observada em ambos os grupos, 4 olhos em uso de CSA apresentaram irritação leve. Em contraste com a terapia de CSA, uma vantagem da ICP é o fato de não depender da colaboração do paciente no armazenamento, o que pode, potencialmente, levar à contaminação, se não feito conforme orientação prévia6.
Mohammed et al. realizaram um estudo com 28 olhos, para comparar a ICP na GL com LA. Esse estudo foi similar ao realizado por Avila et al. uma vez que ambos, incluíram apenas pacientes portadores da DOS severa secundário a SS13. O próprio olho do paciente foi utilizado como grupo controle, ou seja, em um mesmo paciente, um olho recebia ICP enquanto o olho contralateral recebia LA. Após 3 meses a análise mostrou eficácia significativamente superior em favor da ICP22.
DISCUSSÃO
Colírio de soro autólogo (CSA)
O CSA é produzido a partir do próprio sangue do paciente e o mesmo possui similaridade às lágrimas naturais nos seus aspectos bioquímico e epiteliótropico. O seu uso objetiva tratar pacientes refratários ao tratamento convencional para olhos secos ou outras epiteliopatias12. O CSA é obtido através do processo de centrifugação, no qual, o sangue é separado do soro, esse último é então diluído e pode durar até 6 meses quando mantido a -30ºC9. Existe muita discussão sobre qual concentração deve ser utilizada na preparação do CSA, pois o TGF-ß, molécula presente no soro e que possui efeito antiproliferativo23, possui concentração cinco vezes maior que o encontrado na lágrima humana9. A falta de consenso na diluição do CSA leva ao uso, em estudos de tratamento, de formulações que variam sua concentração entre 20% a 100%11.
Colírio de concentrado de plaquetas (CCP)
O CP tem sido utilizado com sucesso no tratamento de patologias em diversos campos da medicina, com destaque na oftalmologia, em cirurgias ortopédicas, maxilofaciais e plástica24.
Injeção de concentrado de plaquetas (ICP)
A ICP é uma terapia utilizada quando se almeja a regeneração de tecidos pela riqueza em fatores de crescimento, que estimulam a proliferação e regeneração de células tronco25. Na oftalmologia ela foi utilizada com sucesso para aumentar a produção da glândula lacrimal (GL) disfuncional, secundário a patologias como a SS22. A GL é crucial para a saúde da superfície ocular, desta forma, patologias que afetam seu funcionamento podem levar a deficiência aquosa e perda da homeostase da superfície ocular26. A lágrima é composta por 3 camadas: a interior composta por mucina, a exterior lipídica e a intermediária aquosa (produzida principalmente na GL), a qual, quando insuficiente, é uma das principais causas da DOS27.
Os estudos mencionados nos resultados abordam diferentes terapêuticas para o tratamento da DOS e suas variações, incluindo o uso de colírios de CSA, colírios de CCP, e ICP. A análise comparativa sugere que a escolha da terapia para o tratamento da DOS pode depender da causa subjacente, gravidade da doença e preferências do paciente. O CSA, CCP e ICP parecem ser opções eficazes em diferentes cenários clínicos, com benefícios específicos para cada um. O uso de CCP autólogo se destacou no tratamento de pacientes diabéticos, enquanto a ICP na glândula lacrimal mostrou ser eficaz em pacientes com DOS severa secundária a SS.
Cada abordagem terapêutica tem suas vantagens e desvantagens, e a escolha deve ser personalizada com base na avaliação clínica do paciente. A pesquisa sobre novos tratamentos para a doença do olho seco aumentou demasiadamente nos últimos anos. A mudança mais significativa é a busca por terapias que possam reverter a etiologia subjacente, como a inflamação e a deficiência aquosa, ao contrário de apenas tratar os sintomas. Terapias inovadoras são opções disponíveis aos pacientes refratários às terapias tradicionais. A meta futura é cada vez mais o refino de terapias que tragam resolução definitiva em detrimento do alívio sintomático transitório.
Apesar da DOS possuir etiologia multifatorial, resultados de ensaios clínicos analisados, sugere que os tratamentos com hemocomponentes e hemoderivados, como CSA, CCP e ICP, são opções promissoras para pacientes com DOS, especialmente aqueles refratários a tratamentos convencionais. A escolha entre essas terapias deve ser individualizada, considerando a etiologia da DOS, a gravidade da condição e as preferências do paciente. Além disso, o desenvolvimento contínuo de terapias inovadoras busca oferecer soluções mais eficazes e duradouras para a DOS, com o objetivo final de resolver as causas subjacentes em vez de apenas aliviar os sintomas temporariamente.
REFERÊNCIAS
1. Yılmaz U, Küçük E, Koç Ç, Gökler E. Comparison of Autologous Serum Versus Preservative Free Artificial Tear in Patients with Dry Eyes Due to Systemic Isotretinoin Therapy. Current Eye Research. 2017;42(6):827-31.
2. Craig JP, Nichols KK, Akpek EK, Caffery B, Dua HS, Joo CK, et al. TFOS DEWS II Definition and Classification Report. The Ocular Surface. 2017;15(3):276-83.
3. Rodríguez Calvo-de-Mora M, Domínguez-Ruiz C, Barrero-Sojo F, Rodríguez-Moreno G, Antúnez Rodríguez C, Ponce Verdugo L, et al. Autologous versus allogeneic versus umbilical cord sera for the treatment of severe dry eye disease: a double-blind randomized clinical trial. Acta Ophthalmologica. 2022;100(2).
4. Celebi ARC, Ulusoy C, Mirza GE. The efficacy of autologous serum eye drops for severe dry eye syndrome: a randomized double-blind crossover study. Graefes Arch Clin Exp Ophthalmol. 2014;252(4):619-26.
5. Yoon KC, Im SK, Park YG, Jung YD, Yang SY, Choi J. Application of Umbilical Cord Serum Eyedrops for the Treatment of Dry Eye Syndrome. Cornea. 2006;25(3):268-72.
6. Allam I. Autologous serum eye drops versus lacrimal gland injection of platelet-rich plasma for severe dry eye. Delta J Ophthalmol. 2021;22(4):251.
7. Noble BA. Comparison of autologous serum eye drops with conventional therapy in a randomised controlled crossover trial for ocular surface disease. British Journal of Ophthalmology. 2004;88(5):647-52.
8. Fox RI, Chan R, Michelson JB, Belmont JB, Michelson PE. Beneficial Effect of Artificial Tears Made with Autologous Serum in Patients with Keratoconjunctivitis Sicca. Arthritis & Rheumatism. 1984;27(4):459-61.
9. Semeraro F, Forbice E, Braga O, Bova A, Di Salvatore A, Azzolini C. Evaluation of the Efficacy of 50% Autologous Serum Eye Drops in Different Ocular Surface Pathologies. BioMed Research International. 2014;2014:1-11.
10. Lee GA, Chen SX. Autologous serum in the management of recalcitrant dry eye syndrome. Clin Exp Ophthalmol. 2008;36(2):119-22.
11. Hwang J, Chung SH, Jeon S, Kwok SK, Park SH, Kim MS. Comparison of Clinical Efficacies of Autologous Serum Eye Drops in Patients With Primary and Secondary Sjögren Syndrome. Cornea. julho de 2014;33(7):663-7.
12. Cho YK, Huang W, Kim GY, Lim BS. Comparison of Autologous Serum Eye Drops with Different Diluents. Current Eye Research. 2013;38(1):9-17.
13. Avila MY, Igua AM, Mora AM. Randomised, prospective clinical trial of platelet-rich plasma injection in the management of severe dry eye. Br J Ophthalmol. 2019;103(5):648-53.
14. Ribeiro MMR, Timbó F, Ribeiro E, Ribeiro LE. The long-term effects of platelet -rich plasma in diabetic dry eye: a series of cases. Revista Brasileira de Oftalmologia. 2019;78(1).
15. Pan Q, Angelina A, Marrone M, Stark WJ, Akpek EK. Autologous serum eye drops for dry eye. Cochrane Eyes and Vision Group, organizador. Cochrane Database of Systematic Reviews. 2017; 2017(2).
16. Ribeiro MVMR, Barbosa FT, Ribeiro LEF, Lacet CMC, Lyra JM de AG, Guedes V de L, et al. Platelet-rich plasma in diabetic dry eye disease. Revista Brasileira de Oftalmologia. 2016;75.
17. Mendes KDS, Silveira RC de CP, Galvão CM. Revisão integrativa: método de pesquisa para a incorporação de evidências na saúde e na enfermagem. Texto contexto - enferm. 2008;17(4):758-64.
18. Jirsova K, Brejchova K, Krabcova I, Filipec M, Al Fakih A, Palos M, et al. The Application of Autologous Serum Eye Drops in Severe Dry Eye Patients; Subjective and Objective Parameters Before and After Treatment. Current Eye Research. 2014;39(1):21-30.
19. Van der Meer PF, Verbakel SK, Honohan Á, Lorinser J, Thurlings RM, Jacobs JFM, et al. Allogeneic and autologous serum eye drops: a pilot double-blind randomized crossover trial. Acta Ophthalmologica. 2021;99(8):837-42.
20. García-Conca V, Abad-Collado M, Hueso-Abancens JR, Mengual-Verdú E, Piñero DP, Aguirre-Balsalobre F, et al. Efficacy and safety of treatment of hyposecretory dry eye with platelet-rich plasma. Acta Ophthalmol. 2019;97(2).
21. Metheetrairut C, Ngowyutagon P, Tunganuntarat A, Khowawisetsut L, Kittisares K, Prabhasawat P. Comparison of epitheliotrophic factors in platelet-rich plasma versus autologous serum and their treatment efficacy in dry eye disease. Sci Rep. 2022;12(1):8906.
22. Avila MY. Restoration of Human Lacrimal Function Following Platelet-Rich Plasma Injection. Cornea. 2014;33(1):18-21.
23. Semeraro F, Forbice E, Nascimbeni G, Taglietti M, Romano V, Guerra G, et al. Effect of Autologous Serum Eye Drops in Patients with Sjögren Syndrome-related Dry Eye: Clinical and In Vivo Confocal Microscopy Evaluation of the Ocular Surface. 2016;30(6):931-8.
24. Panda A, Jain M, Vanathi M, Velpandian T, Khokhar S, Dada T. Topical Autologous Platelet-Rich Plasma Eyedrops for Acute Corneal Chemical Injury. Cornea. 2012;31(9):989-93.
25. Tobita M, Tajima S, Mizuno H. Adipose tissue-derived mesenchymal stem cells and platelet-rich plasma: stem cell transplantation methods that enhance stemness. Stem Cell Res Ther. 2015;6(1):215.
26. Mohammed MA, Allam IY, Shaheen MS, Lazreg S, Doheim MF. Lacrimal gland injection of platelet rich plasma for treatment of severe dry eye: a comparative clinical study. BMC Ophthalmol. 2022;22(1):343.
27. Kawakita T. Regeneration of Lacrimal Gland Function to Maintain the Health of the Ocular Surface. Invest Ophthalmol Vis Sci. 2018;59(14):DES169.
INFORMAÇÃO DOS AUTORES |
|
 |
» Vitor Souza Magalhães https://orcid.org/0000-0003-4308-4390 https://lattes.cnpq.br/8263955563980494 |
 |
» Milena Souza Ribeiro Santos https://orcid.org/0000-0001-5559-5986 https://lattes.cnpq.br/2572273146669592 |
 |
» Marina Viegas Moura Rezende Ribeiro https://orcid.org/0000-0001-7626-2806 https://lattes.cnpq.br/1596177314440842 |
Financiamento: Declaram não haver.
Conflitos de Interesse: Declaram não haver.
Recebido em:
19 de Maio de 2023.
Aceito em:
14 de Junho de 2024.