Isabella Wanderley de Queiroga Evangelista1; Camila Ribeiro Coutinho Honório2; Edivânia Pereira Leite3; Túlio Ivo Cordeiro Eulálio4
DOI: 10.17545/eoftalmo/2018.0014
RESUMO
OBJETIVO: Este estudo objetivou verificar se características morfológicas à tomografia de coerência óptica de domínio espectral afetam os resultados anatômicos na degeneração macular relacionada à idade neovascular tratada com ranibizumabe.
MÉTODOS: Avaliou-se a presença de fluido intrarretiniano, de fluido sub-retiniano, de fluido intrarretiniano associado a fluido sub-retiniano, além de descolamento do epitélio pigmentar da retina, antes do tratamento, e a associação dessas alterações com a ausência de fluido retiniano, após o tratamento. Foram incluídos 22 olhos virgens de tratamento e submetidos a injeções mensais de ranibizumabe.
RESULTADOS: Inicialmente, 22,7% dos olhos apresentavam apenas fluido intrarretiniano (grupo 1), 27,2%, apenas fluido sub-retiniano (grupo 2) e 45,4%, combinação de fluidos intrarretiniano e sub-retiniano (grupo 3). Com o tratamento, os percentuais de olhos que se apresentaram sem fluido foram 66,6, 60,0 e 33,3% para os grupos 1, 2 e 3, respectivamente. Nenhum dos olhos com descolamento do epitélio pigmentar associado às alterações iniciais se apresentou sem fluido após o tratamento.
CONCLUSÃO: Olhos que apresentavam descolamento do epitélio pigmentar inicialmente exibiram a pior resposta anatômica ao tratamento com ranibizumabe. Olhos com a associação de fluidos intrarretiniano e sub-retiniano responderam pior ao tratamento do que aqueles com fluido sub-retiniano ou fluido intrarretiniano como alteração isolada.
Palavras-chave: Degeneração Macular; Ranibizumab; Tomografia de Coerência Óptica.
ABSTRACT
OBJECTIVE: This study aimed to assess whether morphological features observed on spectral domain optical coherence tomography affect anatomical results in patients with neovascular age-related macular degeneration treated with ranibizumab.
METHODS: Before treatment, we assessed the presence of intraretinal fluid, subretinal fluid, an association between both, and retinal pigment epithelial detachment. After treatment, we assessed the association between these changes and the absence of retinal fluid. Twenty-two virgin eyes were included and underwent monthly injections of ranibizumab.
RESULTS: Before treatment, 22.7% of the eyes presented with intraretinal fluid only (group 1), 27.2% exhibited subretinal fluid only (group 2), and 45.4% had a combination of both (group 3). After treatment, 66.6%, 60.0%, and 33.3% of the eyes in groups 1, 2, and 3, respectively, presented no fluid, and none of the eyes with pigment epithelial detachment associated with the initial changes presented no fluid.
CONCLUSION: Eyes with retinal pigment epithelial detachment before treatment had the worst anatomical response to ranibizumab treatment. Eyes with a combination of both intraretinal and subretinal fluids had a worse response to treatment than those with intraretinal or subretinal fluid alone.
Keywords: Macular Degeneration; Ranibizumab; Tomography, Optical Coherence.
RESUMEN
OBJETIVO: Este estudio tuvo como objetivo verificar si las características morfológicas a la tomografía de coherencia óptica de dominio espectral afectan los resultados anatómicos en la degeneración macular relacionada a la edad neovascular tratada con ranibizumab.
MÉTODOS: se ha evaluado la presencia de líquido intrarretiniano, de líquido subretiniano, de líquido intrarretiniano asociado a líquido subretiniano, además de desgarro del epitelio pigmentario retiniano, antes del tratamiento, y la asociación de esas alteraciones con la ausencia de líquido retiniano tras el tratamiento. Fueron incluidos 22 ojos vírgenes de tratamiento y sometidos a inyecciones mensuales de ranibizumab.
RESULTADOS: Inicialmente, el 22,7% de los ojos presentaban solo líquido intrarretiniano (grupo 1), 27,2%, solo líquido subretiniano (grupo 2) y 45,4%, combinación de líquido intrarretiniano y subretiniano (grupo 3). Con el tratamiento, los porcentajes de ojos que se presentaron sin líquido fueron 66,6, 60,0 y 33,3% para los grupos 1, 2 3, respectivamente. Ninguno de los ojos con desgarro del epitelio pigmentario asociado a las alteraciones iniciales se presentó sin fluido tras el tratamiento.
CONCLUSIÓN: Los ojos que presentaban desgarro del epitelio pigmentar inicialmente mostraron la peor respuesta anatómica al tratamiento con ranibizumab. Ojos con la asociación de fluidos intrarretiniano y subretiniano respondieron de peor manera al tratamiento que aquellos con líquido subretiniano o líquido intrarretiniano como alteración separada.
Palabras-clave: Degeneración Macular; Ranibizumab; Tomografía de Coherencia Óptica.
INTRODUÇÃO
O advento da terapia antiangiogênica revolucionou o tratamento da degeneração macular relacionada à idade neovascular (DMRIn), a principal causa de perda definitiva da visão entre a população idosa. Além disso, modernos métodos diagnósticos e de monitoramento, como a tomografia de coerência óptica de domínio espectral (TCO-DE), possibilitaram uma melhor compreensão da doença e dos danos estruturais à mácula por ela causados, contribuindo para decréscimo significativo dos casos de cegueira e melhora da qualidade de vida.
Apesar de todo esse avanço, a classificação da DMRI exsudativa mais amplamente utilizada até hoje ainda é aquela proposta há mais de 20 anos pelo Macula Photocoagulation Study Group1, com base em aspectos da angiografia fluoresceínica. Utilizada com o propósito de determinar quais pacientes seriam beneficiados pela fotocoagulacão com o laser térmico, pretendendo-se, com esse método, a erradicação de todo o complexo neovascular, essa classificação objetivava a precisa delimitação da lesão, determinando sua localização extra, justa ou subfoveal e, de acordo com o padrão da fluorescência, seu caráter “clássico” ou “oculto”. Extremamente útil na era pré antiangiogênica, não possibilitou que fosse mostrada diferença na resposta terapêutica entre esses dois tipos de lesão quando utilizada nos grandes ensaios clínicos ANCHOR e MARINA, que mudaram dramaticamente a expectativa que se tinha acerca da DMRIn2,3.
Entretanto, como clínicos, observamos frequentemente considerável variabilidade nas respostas individuais de pacientes ao tratamento antiangiogênico, o que faz despertar o interesse por explorar e compreender os fatores envolvidos nesses resultados.
O objetivo do presente estudo é verificar se características morfológicas à TCO-DE afetam os resultados anatômicos de olhos portadores de DMRIn tratados com ranibizumabe (Lucentis®, Novartis Pharma Stein AG, Stein, Swiss).
MÉTODOS
Estudo clínico descritivo tipo série de casos em que foram avaliadas características da morfologia macular à TCO-DE antes e após o tratamento com ranibizumabe (Lucentis®). Antes do início do estudo, obteve-se a aprovação do Comitê de Ética local, e todos os procedimentos foram realizados em conformidade com a Declaração de Helsink. Foram incluídos no estudo pacientes com diagnóstico de DMRIn virgens de tratamento. Foram excluídos aqueles com tratamento prévio para a DMRI ou com outras morbidades retinianas associadas, além daqueles que tiveram o primeiro ciclo de tratamento interrompido por razões de qualquer natureza (não comparecimento, falta de acesso ao medicamento etc).
Os pacientes foram submetidos a injeções mensais de ranibizumabe (Lucentis®) até a estabilidade da melhor acuidade visual corrigida (MAVC) por três medidas consecutivas na vigência do tratamento. O equipamento utilizado para o estudo morfológico da mácula foi o Spectralis® (Heidelberg Engineering, Heidelberg, Germany) e foram avaliados os seguintes aspectos: presença de fluido intrarretiniano (FIR; figura 1), presença de fluido subretiniano (FSR; figura 2), presença de FIR associado a FSR (figura 3) e presença de descolamento do epitélio pigmentar da retina (DEP; figura 4) antes do tratamento, e a associação dessas alterações com a ausência de fluido retiniano após o tratamento.
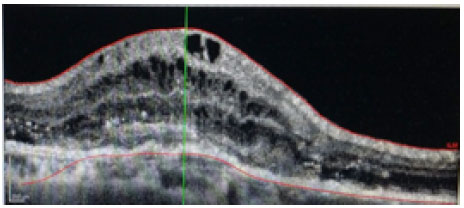
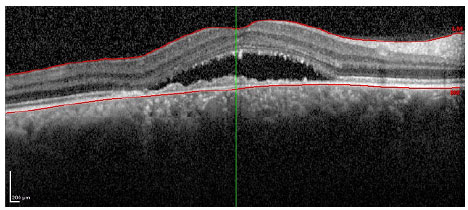
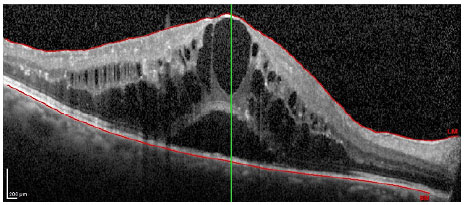
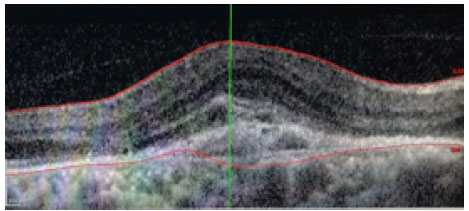
RESULTADOS
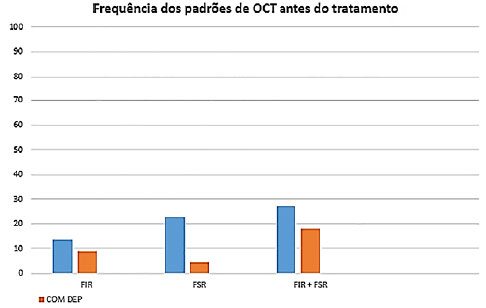
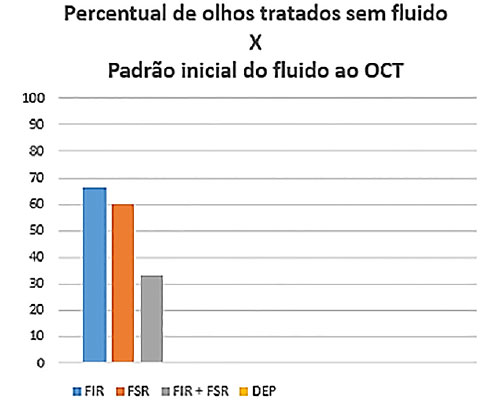
Foram incluídos 22 olhos (21 pacientes) no estudo, sendo a média de idade dos sujeitos de 70,3 anos e a média de injeções de 4,5. Do total, 22,7% dos olhos apresentavam apenas fluido intrarretiniano (grupo 1); 27,2%, apenas fluido sub-retiniano (grupo 2); e 45,4%, combinação de fluidos intrarretiniano e sub-retiniano (grupo 3) (figura 5). Com o tratamento, os percentuais de olhos que se apresentaram sem fluido foram 66,6, 60,0 e 33,3% para os grupos 1, 2 e 3, respectivamente. Nenhum dos olhos com descolamento do epitélio pigmentar associado às alterações iniciais se apresentou sem fluido após o tratamento, independentemente do padrão de fluido que exibia inicialmente: FIR, FSR, e associação de FSR e FIR (figura 6).
DISCUSSÃO
Terapias anti-VEGF provaram reduzir ou reverter a perda de visão de pacientes com DMRIn. Entretanto, por causa da variabilidade das respostas em diferentes pacientes e das flutuações nas respostas de um mesmo paciente, preditores para os resultados do tratamento anti-VEGF têm sido investigados4,5.
Características genéticas, demográficas e clínicas têm sido associadas na literatura com a resposta à terapia antiangiogênica para a DMRIn6,7,8. Aspectos morfológicos da TCO também foram propostos como base para uma nova classificação da doença9. Evidentemente, há muitas vantagens da utilização da TCO-DE para melhorar a acurácia do prognóstico para a degeneração macular relacionada à idade: é um método rápido, não invasivo e que já faz parte da propedêutica da doença.
O nosso estudo investigou se características da TCO da linha de base são capazes de diferenciar respostas anatômicas ao primeiro ciclo de tratamento com ranibizumabe (Lucentis®). Na amostra estudada, a presença de DEP inicial se associou à persistência de fluido retiniano em todos os casos. A associação de FIR e FSR na linha de base também se correlacionou a piores respostas ao tratamento quando comparada com a presença de um ou outro padrão de fluido como alteração isolada.
Há algumas limitações relacionadas ao desenho do nosso estudo: pequeno, não randomizado, retrospectivo e com um tempo de seguimento limitado. Além disso, variáveis genéticas e demográficas e a associação dos aspectos morfológicos com os resultados funcionais também poderiam ter sido estudadas. Entretanto, é um dos poucos estudos da literatura envolvendo a estrutura macular e a reposta terapêutica em pacientes com DMRIn.
Olhos com degeneração macular relacionada à idade exsudativa que apresentaram DEP inicialmente exibiram a pior resposta anatômica ao tratamento com ranibizumabe (Lucentis®). Olhos com a associação de FIR e FSR responderam pior ao tratamento com esse fármaco do que aqueles com apenas FIR ou FSR como alteração isolada.
REFERÊNCIAS
1. Argon laser photocoagulation for neovascular maculopathy. Five-year results from randomized clinical trials. Macular Photocoagulation Study Group. Arch Ophthalmol. 1991;109(8):1109-14.
2.Brown DM, Kaiser PK, Michels M, Soubrane G, Heier JS, Kim RY, et al.; ANCHOR Study Group. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med. 2006;355(14):1432-44.
3.Rosenfeld PJ, Brown DM, Heier JS, Boyer DS, Kaiser PK, Chung CY, et al.; MARINA Study Group. Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355(14):1419-31.
4.Ying GS, Maguire MG, Daniel E, Ferris FL, Jaffe GJ, Grunwald JE, et al.; Comparison of Age-Related Macular Degeneration Treatments Trials (CATT) Research Group. Association of Baseline Characteristics and Early Vision Response with 2-Year Vision Outcomes in the Comparison of AMD Treatments Trials (CATT). Ophthalmology. 2015;122(12):2523-31.e1.
5.Ying GS, Huang J, Maguire MG, Jaffe GJ, Grunwald JE, Toth C, et al.; Comparison of Age-related Macular Degeneration Treatments Trials Research Group. Baseline predictors for one-year visual outcomes with ranibizumab or bevacizumab for neovascular age-related macular degeneration. Ophthalmology. 2013;120(1):122-9.
6.Krishnan R, Arora R, De Salvo G, Stinghe A, Severn PS, Pal B, et al. Vitreomacular traction affects anti-vascular endothelial growth factor treatment outcomes for exudative age-related macular degeneration. Retina. 2015;35(9):1750-6.
7.Brantley MA Jr, Fang AM, King JM, Tewari A, Kymes SM, Shiels A. Association of complement factor H and LOC387715 genotypes with response of exudative age-related macular degeneration to intravitreal bevacizumab. Ophthalmology. 2007;114(12):2168-73.
8.Smailhodzic D, Muether PS, Chen J, Kwestro A, Zhang AY, Omar A, et al. Cumulative effect of risk alleles in CFH, ARMS2, and VEGFA on the response to ranibizumab treatment in age-related macular degeneration. Ophthalmology. 2012;119(11):2304-11.
9.Freund KB, Zweifel SA, Engelbert M. Do we need a new classification for choroidal neovascularization in age-related macular degeneration? Retina. 2010;30(9):1333-49.



Fonte de financiamento: declaram não haver.
Parecer CEP: CAAE: 50979415.6.0000.5183 (Hospital Universitário Lauro Wanderley/UFPB).
p>Conflito de interesses: declaram não haver.
Recebido em:
15 de Maio de 2018.
Aceito em:
25 de Maio de 2018.