Leonardo Luis Cassoni; Isabela Franco Villela; Francyne Veiga Reis Cyrino
DOI: 10.17545/eOftalmo/2026.v12.005
RESUMO
A endoftalmite é uma infecção intraocular rara e grave, geralmente causada por patógenos bacterianos ou fúngicos. Pode apresentar-se de forma endógena, originada de infecções sistêmicas, ou exógena, associada a trauma ou procedimentos cirúrgicos oculares. Cerca de 5% a 10% dos casos de endoftalmite são endógenos, resultantes da disseminação hematogênica de microrganismos que ultrapassam a barreira hemato-ocular. Indivíduos imunocomprometidos apresentam risco aumentado de endoftalmite endógena, frequentemente relacionada à translocação de microrganismos da própria microbiota. Este relato descreve um caso de endoftalmite endógena ocorrido durante o isolamento social da pandemia de COVID-19, após infecção por SARS-CoV-2. O objetivo é apresentar a manifestação clínica, o manejo terapêutico e os desfechos anatômicos e visuais, além de discutir possíveis associações entre infecções oculares e a COVID-19, sem estabelecer relação causal direta.
Palavras-chave: Endoftalmite endógena; Staphylococcus hominis; COVID-19; Relato de caso; Infecção ocular.
ABSTRACT
Endophthalmitis is a rare but severe intraocular infection, typically caused by bacterial or fungal pathogens. It may present as an endogenous infection, originating from systemic infections, or an exogenous one, associated with ocular trauma or surgical procedures. Approximately 5%–10% of cases involve endogenous endophthalmitis, which is caused by the hematogenous dissemination of microorganisms that cross the blood–ocular barrier. Immunocompromised individuals are at increased risk of endogenous endophthalmitis attributed to the translocation of microorganisms from their own microbiota. Herein, we report a patient who developed endogenous endophthalmitis during social isolation in the coronavirus disease 2019 (COVID-19) pandemic, after severe acute respiratory syndrome coronavirus 2 infection. This report aimed to describe the clinical presentation, management, and anatomical and visual outcomes of endogenous endophthalmitis, and to discuss potential associations between ocular infections and COVID-19, without implying direct causality.
Keywords: Endogenous endophthalmitis; Staphylococcus hominis; COVID-19; Case report; Eye infection.
INTRODUÇÃO
A endoftalmite é uma infecção intraocular rara e potencialmente devastadora, que acomete as estruturas internas do globo ocular. Geralmente causada por bactérias ou fungos, pode ser classificada como endógena — quando decorrente de infecção sistêmica — ou exógena, quando relacionada a trauma ou cirurgia ocular.
Estima-se que entre 5% e 10% dos casos de endoftalmite sejam do tipo endógeno (EE), situação na qual microrganismos provenientes de focos infecciosos à distância alcançam a circulação sistêmica e atravessam a barreira hemato-ocular1-4. Os principais sítios primários descritos incluem o trato urinário, o sistema hepatobiliar e dispositivos intravasculares, como cateteres1,4. Pacientes imunocomprometidos são particularmente suscetíveis, uma vez que a EE pode resultar da translocação de microrganismos da própria microbiota.
Neste relato, apresentamos um caso de EE ocorrido durante o isolamento social imposto pela pandemia de COVID-19, após infecção confirmada por SARS-CoV-2. São descritas as manifestações clínicas, a abordagem terapêutica e os desfechos funcionais e anatômicos, além de uma discussão sobre possíveis associações entre infecções oculares e a COVID-19, de forma cautelosa e baseada em hipóteses.
RELATO DE CASO
Paciente masculino, 65 anos, foi encaminhado ao nosso serviço com queixa de baixa visual progressiva e indolor no olho direito (OD), com evolução de aproximadamente dois meses. Negava trauma ou cirurgia ocular prévia. Relatou internação hospitalar prévia por COVID-19, durante a qual apresentou colelitíase e foi submetido à colecistectomia, além de tratamento para infecção do trato urinário. Quinze dias após a alta hospitalar, iniciou quadro de moscas volantes no OD.
Procurou atendimento oftalmológico, sendo observada reação de câmara anterior e vitrite. Foi instituído tratamento com sulfametoxazol-trimetoprim (800/160 mg, duas vezes ao dia), prednisolona acetato 1% tópica e tropicamida 1%, mantido por cerca de dois meses, sem melhora visual. Posteriormente, foi encaminhado ao nosso serviço para investigação. Como antecedentes pessoais, apresentava hipertensão arterial sistêmica e diabetes mellitus.
Ao exame oftalmológico, o OD apresentava percepção luminosa, injeção ciliar, reação de câmara anterior graduada como 2+ com fibrina, sinéquias posteriores em 360º e catarata nuclear 2+. O segmento posterior não pôde ser avaliado devido à opacificação vítrea densa. No olho esquerdo (OE), a acuidade visual era de 20/20, sem sinais inflamatórios. As pressões intraoculares eram de 11 mmHg no OD e 12 mmHg no OE.
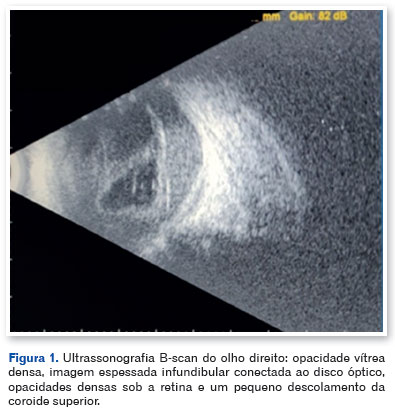
A ultrassonografia modo B evidenciou opacidade vítrea densa, imagem espessada em forma de funil conectada ao disco óptico, opacidades sub-retinianas e pequeno descolamento coroidal superior (Figura 1). Foi realizada paracentese de humor aquoso, com reação em cadeia da polimerase (PCR) negativa para Toxoplasma gondii, Cytomegalovirus, Herpes simplex tipo 1 e Varicella zoster. Diante da hipótese de pan-uveíte de etiologia indeterminada, indicou-se vitrectomia diagnóstica.
O procedimento cirúrgico incluiu coleta de vítreo para culturas bacteriana e fúngica, seguida de liberação de sinéquias, vitrectomia via pars plana, endolaser e tamponamento com óleo de silicone. Foram administrados antibióticos intravítreos (ceftazidima, anfotericina B e vancomicina). Amostras vítreas foram encaminhadas para cultura, teste de sensibilidade antimicrobiana e PCR.
Durante a cirurgia, além de vitrite intensa, observou-se descolamento total de retina com fluido sub-retiniano espesso. Um fragmento retiniano foi coletado para exame anatomopatológico. O PCR vítreo foi negativo para os agentes testados; entretanto, a cultura revelou crescimento de Staphylococcus hominis subsp. hominis, confirmando o diagnóstico de endoftalmite endógena. Apesar do tratamento instituído, o desfecho visual foi desfavorável.
DISCUSSÃO
Os estafilococos coagulase-negativos (CoNS), como Staphylococcus epidermidis e Staphylococcus saprophyticus, são componentes comuns da microbiota da superfície ocular e representam os agentes mais frequentemente associados à endoftalmite pós-procedimento2. Staphylococcus hominis, também pertencente ao grupo dos CoNS, integra a microbiota cutânea e das mucosas humanas e pode apresentar prevalência superior à de S. epidermidis em indivíduos saudáveis, embora permaneça como causa incomum de endoftalmite3-7.
O potencial patogênico dos CoNS está intimamente relacionado à sua capacidade de formar biofilmes, o que facilita a adesão tanto a superfícies biológicas, como a conjuntiva, quanto a materiais inertes, incluindo dispositivos médicos e cateteres8. Pacientes com diabetes mellitus apresentam maior formação de biofilme conjuntival, o que pode contribuir para aumento da suscetibilidade a infecções7-9. Além disso, infecções por CoNS são mais frequentemente observadas em indivíduos imunocomprometidos e na presença de corpos estranhos ou comorbidades sistêmicas5,6.
Durante a pandemia de COVID-19, diversos relatos descreveram casos de endoftalmite endógena ocorrendo em associação temporal com a infecção por SARS-CoV-2. Esses casos foram observados tanto durante a hospitalização quanto no período pós-infeccioso, frequentemente em pacientes com comorbidades sistêmicas, infecções recentes ou desequilíbrio imunológico10. É importante ressaltar que tais observações sustentam uma associação, e não uma relação causal direta.
Além dos efeitos virais diretos, o próprio contexto da pandemia esteve associado a fatores que podem aumentar indiretamente a suscetibilidade a infecções secundárias, incluindo redução da atividade física, atraso no acesso a cuidados médicos especializados e uso inadequado de antimicrobianos11-13. Esses fatores podem contribuir para maior vulnerabilidade sistêmica, especialmente em pacientes com doenças crônicas.
Do ponto de vista fisiopatológico, diversos órgãos — como rins e trato gastrointestinal — apresentam maior expressão da enzima conversora de angiotensina 2 (ECA2), principal receptor de entrada celular do SARS-CoV-214,15. A infecção viral desses órgãos pode resultar em disfunção transitória ou persistente, potencialmente contribuindo para desequilíbrio imunológico durante a fase de recuperação16. Tal desregulação imune pós-viral tem sido hipotetizada como possível fator predisponente a infecções oportunistas, incluindo a endoftalmite endógena, embora esse mecanismo permaneça especulativo.
No presente caso, o paciente desenvolveu endoftalmite endógena após infecção por COVID-19, infecção do trato urinário e colecistite com necessidade de colecistectomia. Embora um desequilíbrio imunológico pós-infeccioso relacionado ao SARS-CoV-2 possa ser considerado como fator contribuinte, essa hipótese deve ser interpretada com cautela. Ressalta-se que o diabetes mellitus, isoladamente, constitui fator de risco bem estabelecido para infecções por CoNS e pode explicar de forma independente a ocorrência de endoftalmite endógena neste paciente8,17. Ainda assim, a associação temporal com a COVID-19 e as complicações sistêmicas subsequentes reforçam a importância de vigilância clínica rigorosa em indivíduos vulneráveis.
Em conclusão, embora o isolamento social tenha sido essencial para mitigar a disseminação da COVID-19, ele foi acompanhado por consequências não intencionais, incluindo redução da atividade física, atrasos no acesso aos cuidados médicos e alterações no equilíbrio da microbiota do hospedeiro11-13. Além disso, a COVID-19 tem sido associada a efeitos sistêmicos e à desregulação imunológica transitória, o que pode aumentar a suscetibilidade a infecções secundárias, particularmente em pacientes imunocomprometidos14-16.
Este caso destaca a importância de considerar patógenos oportunistas, como Staphylococcus hominis, no diagnóstico diferencial da endoftalmite endógena, especialmente em pacientes com múltiplos fatores de risco sistêmicos. Embora não seja possível estabelecer uma relação causal direta com a infecção por SARS-CoV-2, a associação temporal e as complicações sistêmicas observadas justificam investigações adicionais.
CONTRIBUIÇÃO DOS AUTORES:
Contribuição significativa para concepção e design: Leonardo Luis Cassoni. Obtenção dos dados: Leonardo Luis Cassoni. Análise e interpretação dos dados: Leonardo Luis Cassoni. Elaboração do manuscrito: Leonardo Luis Cassoni, Isabela Franco Villela. Revisão significativa do conteúdo intelectual do manuscrito: Francyne Veiga Reis Cyrino, Isabela Franco Villela. Aprovação final ao manuscrito submetido: Leonardo Luis Cassoni, Francyne Veiga Reis Cyrino, Isabela Franco Villela. Análise estatística: Leonardo Luis Cassoni. Obtenção de financiamento: não aplicável. Supervisão de apoio administrativo, técnico ou material: Francyne Veiga Reis Cyrino. Líder do grupo de pesquisa: Francyne Veiga Reis Cyrino.
REFERÊNCIAS
1. Bohigian GM, Olk RJ. Factors associated with a poor visual result in endophthalmitis. Am J Ophthalmol 1986;101(3):332-41.
2. Puliafito CA, Baker AS, Haaf J, Foster CS. Infectious endophthalmitis. Review of 36 cases. Ophthalmology. 1982;89(8):921-929.
3. Shrader SK, Band JD, Lauter CB, Murphy P. The clinical spectrum of endophthalmitis: incidence, predisposing factors, and features influencing outcome. J Infect Dis 1990;162(1):115-120.
4. Jackson TL, Paraskevopoulos T, Georgalas I. Systematic Review Of 342 Cases Of Endogenous Bacterial Endophthalmitis. Surv Ophthalmol. 2014;59(6):627-35.
5. Piette A, Verschraegen G. Role of coagulase-negative staphylococci in human disease. Vet Microbiol. 2009;134(1-2):45-54.
6. Yu W, Kim HK, Rauch S, Schneewind O, Missiakas D. Pathogenic conversion of coagulase-negative staphylococci. Microbes Infect. 2017;19(2):101-109.
7. Gautam V, Sethuraman N, Kaur R, Sachdev S, Marwaha N, Ray P. Changing epidemiology of coagulase-negative staphylococci in normal flora of skin. Indian J Med Microbiol. 2017;35(2):277-278.
8. Kıvanç SA, Arık G, Akova-Budak B, Kıvanç M. Biofilm forming capacity and antibiotic susceptibility of Staphylococcus spp. with the icaA/icaD/bap genotype isolated from ocular surface of patients with diabetes. Malawi Med J. 2018;30(4):243-9.
9. Natsis, NE, Cohen, PR. Coagulase-Negative Staphylococcus Skin and Soft Tissue Infections. Am J Clin Dermatol. 2018;19(5):671-677.
10. Verma S, Walinjkar JA. A case of endogenous endophthalmitis in COVID 19 pandemic. Apollo Med. 2020;17(3):229-32.
11. Goethals L, Barth N, Guyot J, Hupin D, Celarier T, Bongue B. Impact of home quarantine on physical activity among older adults living at home during the COVID-19 pandemic: Qualitative interview study. J Med Internet Res. 2020;22(5):1-5.
12. Wallis CJD, Catto JWF, Finelli A, Glaser AW, Gore JL, Loeb S, et al. The Impact of the COVID-19 Pandemic on Genitourinary Cancer Care: Re-envisioning the Future. Eur Urol. 2020;78(5):731-742.
13. Zhang A, Hobman EV, De Barro P, Young A, Carter DJ, Byrne M. Self-Medication with Antibiotics for Protection against COVID-19: The Role of Psychological Distress, Knowledge of, and Experiences with Antibiotics. Antibiotics (Basel). 2021;10(3):232.
14. Zou X, Chen K, Zou J, Han P, Hao J, Han Z. Single-cell RNA-seq data analysis on the receptor ACE2 expression reveals the potential risk of different human organs vulnerable to 2019-nCoV infection. Front Med. 2020;14(2):185-192.
15. Lin L, Jiang X, Zhang Z, Huang S, Zhang Z, Fang Z, et al. Gastrointestinal symptoms of 95 cases with SARS-CoV-2 infection. Gut. 2020;69(6):997-1001.
16. Balachandar V, Mahalaxmi I, Subramaniam M, Kaavya J, Senthil Kumar N, Laldinmawii G, et al. Follow-up studies in COVID-19 recovered patients - is it mandatory? Sci Total Environ. 2020 Aug 10;729:139021.
17. Armstrong DG, Lanthier J, Lelievre P, Edelson GW. Methicillin-resistant coagulase-negative staphylococcal osteomyelitis and its relationship to broad-spectrum oral antibiosis in a predominantly diabetic population. J Foot Ankle Surg. 1995;34(6):563-6.
| INFORMAÇÃO DOS AUTORES |
|
 |
» Leonardo Luis Cassoni https://orcid.org/0000-0003-1427-9105 http://lattes.cnpq.br/4681844858936626 |
 |
» Francyne Veiga Reis Cyrino https://orcid.org/0000-0002-1892-6210 http://lattes.cnpq.br/0720130883701897 |
 |
» Isabela Franco Villela https://orcid.org/0000-0002-1736-6717 http://lattes.cnpq.br/7786081137581336 |
Financiamento: Declaram não haver.
Aprovado pelo seguinte comitê de ética em pesquisa: Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto – USP – HCFMRP/USP (CAAE: 91209825.6.0000.5440).
Conflitos de Interesse: Declaram não haver.
Recebido em:
10 de Janeiro de 2026.
Aceito em:
11 de Fevereiro de 2026.