Glaycielli Pereira Santos Mandaro de Assis1,2; Paula Yuri Sacai1,2; Andressa Quércia1; Evelyn Benyhe1; Milena Leal Borges1; Sung Eun Song Watanabe1,2
DOI: 10.17545/eOftalmo/2025.0010
RESUMO
A atrofia macular extensa com pseudodrusas é uma degeneração macular progressiva que apresenta amplo espectro de diagnósticos diferenciais. Por se tratar de uma entidade relativamente recente e com fisiopatologia ainda não completamente elucidada, presume-se que muitos casos permaneçam subdiagnosticados, sugerindo que sua prevalência possa ser superior à atualmente descrita na literatura. O presente relato de caso descreve o acompanhamento clínico e funcional ao longo de 11 anos. Inicialmente, o paciente recebeu o diagnóstico de degeneração macular relacionada à idade. Contudo, com o avanço do conhecimento sobre a atrofia macular extensa com pseudodrusas e sua melhor caracterização clínica e por imagem, o quadro mostrou-se compatível com essa entidade. O seguimento prolongado possibilitou a documentação minuciosa da evolução anatômica e funcional da retina ao longo do tempo.
Palavras-chave: Atrofia macular extensa com pseudodrusas; Análise multimodal; Eletrofisiologia da retina; Degeneração macular relacionada à idade.
ABSTRACT
Extensive macular atrophy with pseudodrusen is defined as progressive macular degeneration with a broad spectrum of differential diagnoses. As a recently described entity with an unclear pathophysiology, numerous cases are presumed to remain underdiagnosed, suggesting that its prevalence is higher than the current reports in the literature. The present case report describes an 11-year clinical and functional follow-up. The patient was initially diagnosed with age-related macular degeneration. However, with the improved knowledge on extensive macular atrophy with pseudodrusen and the enhanced characterization of clinical and imaging features, the findings proved to be consistent with this entity. Long-term follow-up enabled detailed documentation of the anatomical and functional retinal changes over time.
Keywords: Extensive macular atrophy with pseudodrusen; Multimodal imaging; Retinal electrophysiology; Age-related macular degeneration.
INTRODUÇÃO
A atrofia macular extensa com pseudodrusas (EMAP) é uma entidade clínica caracterizada pela tríade de atrofia macular com predomínio no eixo vertical, presença de pseudodrusas e áreas periféricas de degeneração tipo pavingstone, geralmente bilateral e simétrica1. Trata-se de uma condição progressiva, associada a comprometimento estrutural e funcional da retina ao longo do tempo.
Estudos subsequentes demonstraram que a doença pode ser complicada pelo desenvolvimento de membrana neovascular sub-retiniana, evento que pode contribuir para piora visual e modificar sua apresentação clínica2. Desde sua descrição inicial como uma entidade distinta3, investigações longitudinais têm caracterizado seu padrão de progressão e o impacto funcional ao longo do tempo4,5.
O diagnóstico da atrofia macular extensa com pseudodrusas pode ser desafiador na prática clínica, especialmente em pacientes em faixas etárias semelhantes às da degeneração macular relacionada à idade. Relatos com seguimento prolongado contribuem para a melhor compreensão da história natural da doença e de suas específicas manifestações estruturais e funcionais.
Este relato de caso descreve a evolução da atrofia coriorretiniana progressiva e o seguimento clínico e funcional do paciente ao longo dos anos, enfatizando a importância da análise multimodal dessa entidade.
RELATO DO CASO
Paciente masculino, 58 anos, procurou atendimento oftalmológico em 2014 com queixa de nictalopia progressiva, acompanhada de piora gradual da acuidade visual (AV) em ambos os olhos (AO), de forma simétrica, principalmente para visão de longe. Negava antecedentes oftalmológicos. Na história patológica pregressa, o paciente relatava episódio de febre reumática aos nove anos de idade, tendo realizado profilaxia secundária com penicilina benzatina até os 18 anos. Adicionalmente, apresentava antecedente de fasciíte necrosante no pós-operatório de apendicectomia e diagnóstico de hérnia de hiato. Negava outras comorbidades sistêmicas relevantes.
O exame inicial mostrou AV de 20/16 no olho direito (OD) e 20/32 no olho esquerdo (OE). O segmento anterior e o corpo vítreo não apresentavam alterações iniciais. O mapeamento de retina evidenciou, bilateralmente pseudodrusas predominantemente entre as arcadas temporais e degeneração tipo pavingstone em periferia (Figura 1). A tomografia de coerência óptica (OCT) revelou depósitos drusiformes sub-retinianos hiper-refletivos. O eletrorretinograma de campo total (ERG CT) indicou disfunção retiniana difusa com comprometimento predominante de bastonetes, embora também com redução da resposta de cones. O eletrorretinograma multifocal (ERG mf) demonstrou perda macular significativa da função de cones, bilateral e simétrica, apesar da discreta assimetria da AV, sugerindo disfunção funcional precedendo as alterações estruturais. Diante desse conjunto de achados, estabeleceu-se inicialmente o diagnóstico de degeneração macular relacionada à idade (DMRI).
Durante o seguimento, o paciente relatava oscilações da AV, intensificação da nictalopia, piora da visão de perto e início de fotofobia. Em 2017, observou-se progressão das pseudodrusas, agora distribuídas de forma mais difusa pelo polo posterior. Apesar do curso gradativo, em 2018 ocorreu piora súbita da visão no OD, cuja AV caiu para 20/200 (OE 20/40). Identificou-se membrana neovascular sub-retiniana (MNVSR) no OD, tratada com injeções intravítreas de anti-VEGF.
Na avaliação de 2020, observou-se áreas de atrofia coriorretiniana central em AO e fibrose sub-retiniana no OD, acompanhadas de expansão centrípeta da degeneração tipo pavingstone. A autofluorescência (Figura 2) mostrou hipoautofluorescência macular bem delimitada e simétrica, com pequena ilha central de hiperautofluorescência no OD e extensa área periférica de hiperautofluorescência em AO, compatível com sofrimento do epitélio pigmentar da retina (EPR). O OCT revelou confluência e espessamento dos depósitos drusiformes sub-retinianos hiper-refletivos, com separação progressiva entre a membrana de Bruch e o EPR.
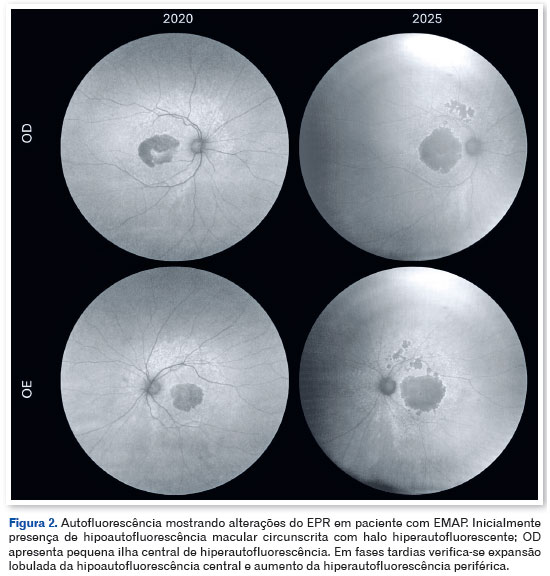
Na última avaliação, em 2025, o paciente referia queda acentuada da AV — 20/320 no OD e 20/40 no OE — acompanhada de escotoma central, discromatopsia, fotofobia intensa com necessidade de filtros ópticos, piora da sensibilidade ao contraste e redução progressiva do campo visual. O mapeamento de retina evidenciou expansão da atrofia coriorretiniana em padrão lobulado, ultrapassando as arcadas, e progressão da degeneração tipo pavingstone. A autofluorescência demonstrou ampla expansão da hipoautofluorescência central e aumento do perímetro de hiperautofluorescência periférica, caracterizando o trajeto evolutivo da doença. O OCT (Figura 3) revelou desorganização das camadas externas da retina, com ruptura da membrana limitante externa, zona elipsóide e zona de interdigitação, culminando em atrofia completa do EPR e retina externa (cRORA).
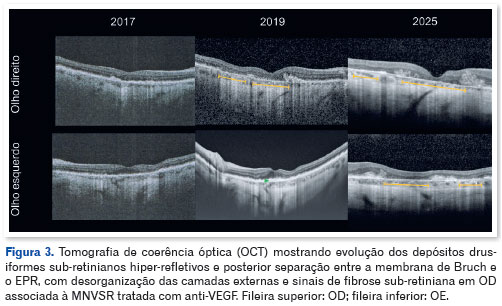
Os exames eletrofisiológicos mostraram gradativa deterioração da função global de bastonetes e cones no ERG CT (Figura 4) e piora da função macular de cones no ERG mf (Figura 5).
DISCUSSÃO
Os sintomas de nictalopia, fotofobia e discromatopsia são característicos do EMAP. Inicialmente, este caso foi interpretado como DMRI precoce4, sendo iniciada suplementação vitamínica conforme o protocolo AREDS 2.
Entretanto, a idade precoce de início, a nictalopia severa, a rápida e progressiva deterioração da função retiniana observada no ERG CT desde o início dos sintomas, a presença de pseudodrusas observada na biomicroscopia de fundo e caracterizadas no OCT5,6 somado à discrepância entre sintomas e achados anatômicos levaram à reconsideração diagnóstica. Conforme Watanabe et al.7, a presença de febre reumática prévia e a tríade clássica do EMAP reforçaram a diferenciação diagnóstica com a DMRI.
Este caso salienta dois aspectos relevantes para a compreensão fisiopatológica do EMAP. O primeiro refere-se a dissociação clínico-funcional: apesar da nictalopia marcante e da queixa subjetiva de piora visual, a acuidade visual inicial permaneceu relativamente preservada embora o ERG CT já evidenciasse perda funcional da retina, e mesmo em fases avançadas, o OE — que não desenvolveu MNVSR — manteve AV de 20/40, apesar da severa degradação da função retiniana observada nos exames eletrofisiológicos, sugerindo que a acuidade visual não é um marcador sensível para estratificar o acometimento retiniano no EMAP. O segundo diz respeito à dissociação entre função e estrutura. Nas fases iniciais, os exames eletrofisiológicos revelaram comprometimento retiniano difuso apesar de alterações anatômicas predominantemente centrais e em fases avançadas, mesmo com a progressão da atrofia coriorretiniana e da degeneração tipo pavingstone, mantinham-se áreas periféricas estruturalmente preservadas; entretanto, a eletrofisiologia demonstrava perda funcional ampla e generalizada.
Desde 2018, a International Society for Clinical Electrophysiology of Vision (ISCEV) padronizou um teste eletrofisiológico chamado de resposta fotópica negativa/photopic negative response (PhNR), que avalia a função das células ganglionares da retina8. Watanabe et al. sugerem que a disfunção de células ganglionares pode constituir um dos achados eletrofisiológicos mais precoces na EMAP9, ampliando o entendimento da fisiopatologia e sugerindo possível envolvimento mais amplo das camadas internas da retina. A inclusão desse protocolo pode se tornar uma ferramenta para o diagnóstico precoce e aprimorar a estratificação funcional do EMAP.
São necessários estudos com amostras maiores e seguimento prolongado para padronizar protocolos multimodais de acompanhamento, definir estágios evolutivos e orientar estratégias terapêuticas específicas para o EMAP.
Concluíndo, a presença de história pregressa de febre reumática e/ou o início precoce e progressivo de degeneração retiniana devem despertar a suspeita diagnóstica de EMAP.
O acompanhamento multimodal permitiu documentar objetivamente as alterações estruturais e funcionais da retina e mácula desde fases iniciais, evidenciando a progressão do acometimento retiniano até a atrofia coriorretiniana. O padrão de disfunção ampla de bastonetes e cones observado no ERG CT associado ao comprometimento macular de cones no mf ERG reforça o entendimento do EMAP como uma doença difusa da retina.
Esses achados reforçam o papel fundamental da avaliação multimodal — integrando exames de imagem de alta resolução e testes eletrofisiológicos — para o diagnóstico, o acompanhamento evolutivo e o manejo clínico adequado dos pacientes com EMAP.
REFERÊNCIAS
1. Antropoli A, Arrigo A, Bianco L, Berni A, Lamberto F, Saladino A, et al. Quantitative multimodal imaging of extensive macular atrophy with pseudodrusen and geographic atrophy with diffuse trickling pattern. Sci Rep. 2023;13(1):1822.
2. Trinco A, Antropoli A, Bianco L, Zaffalon C, Airaldi M, Lanzani A, et al. Incidence, Characteristics, and Outcomes of Macular Neovascularization in Extensive Macular Atrophy with Pseudodrusen-like Appearance. Retina. 2025;45(9):1689-700.
3. Hamel CP, Meunier I, Arndt C, Salah SB, Lopez S, Bazalgette C, et al. Extensive macular atrophy with pseudodrusen-like appearance: a new clinical entity. Am J Ophthalmol. 2009; 147(4):609-20.
4. Antropoli A, Bianco L, Condroyer C, Antonio A, Navarro J, Dagostinoz D, et al. Extensive macular atrophy with pseudodrusen-like appearance: progression kinetics and late-stage findings. Ophthalmology. 2024;131(10):1175-1184.
5. Romano F, Airaldi M, Cozzi M, Oldani M, Riva E, Bertoni AI, et al. Progression of atrophy and visual outcomes in extensive macular atrophy with pseudodrusen-like appearance. Ophthalmol Sci. 2021;1(1):100016.
6. Romano F, Cozzi M, Salvetti AP. Multimodal imaging of extensive macular atrophy with pseudodrusen-like appearance. Ophthalmol Retina. 2023;7(4):332.
7. Watanabe SES, Quercia AZF, Sacai PY. Electrophysiological findings in extensive macular atrophy with pseudodrusen. Doc Ophthalmol. 2023;147(2):121-130.
8. Frishman L, Sustar M, Kremers J, McAnany JJ, Sarossy M, Tzekov R, et al. ISCEV extended protocol for the photopic negative response (PhNR) of the full-field electroretinogram. Doc Ophthalmol. 2018;136(3):207-211.
9. Watanabe SES, Quercia AZF, de Assis GPSM, Borges ML, Sacai PY. Ganglion cell function loss in extensive macular atrophy with pseudodrusen. Int Ophthalmol. 2025;45(1):338.
INFORMAÇÃO DOS AUTORES
Financiamento: Declaram não haver.
Conflitos de interesse: Declaram não haver.
Aprovado pelo seguinte comitê de ética: Universidade Federal de São Paulo (CAAE 73378423.0.0000.5505).
Recebido em:
5 de Janeiro de 2026.
Aceito em:
9 de Janeiro de 2026.