Carlos Eduardo R. Velos; Márcio B. Nehemy
DOI: 10.17545/eOftalmo/2023.0010
RESUMO
A vasculopatia polipoidal da coroide é um subtipo da degeneração macular relacionada à idade cujo tratamento geralmente envolve o uso de agentes anti-VEGF associados ou não à terapia fotodinâmica. O presente caso demonstra o uso do brolucizumabe em um caso de vasculopatia polipoidal da coroide resistente a outros agentes anti-VEGF proporcionando excelente resposta anatômica e funcional.
Palavras-chave: Degeneração macular exsudativa; Fator de crescimento do endotélio vascular; Tomografia de coerência óptica.
ABSTRACT
Polypoidal choroidal vasculopathy is a subtype of age-related macular degeneration whose treatment usually involves the use of anti-vascular endothelial growth factor agents, which may be associated with photodynamic therapy. The current case report demonstrates the use of brolucizumab in a patient with polypoidal choroidal vasculopathy resistant to other anti-vascular endothelial growth factor agents, providing excellent anatomical and functional responses.
Keywords: Exudative macular degeneration; Vascular endothelial growth factor; Optical coherence tomography.
INTRODUÇÃO
A vasculopatia polipoidal da coroide (VPC) pode ser considerada um subtipo da degeneração macular relacionada à idade (DMRI) neovascular caracterizada por neovascularização de coroide do tipo 1 associada a uma rede vascular ramificada com dilatações aneurismáticas1. A angiografia com indocianina verde (AICV) continua sendo o método diagnóstico padrão-ouro, mas a tomografia de coerência óptica (OCT) é um recurso propedêutico mais amplamente disponível e cujos achados, como o descolamento do epitélio pigmentar da retina em U invertido, podem ser bastante sugestivos2,3. Classicamente referida como tendo maior frequência em asiáticos, a VPC também tem alta prevalência no Brasil. Um estudo realizado em pacientes brasileiros portadores de DMRI neovascular mostrou que 24,5% dos pacientes apresentavam esta forma da doença4. O tratamento atual da VPC envolve o uso de agentes anti-VEGF associados ou não à PDT. Hemorragias sub-retinianas recorrentes e acúmulo persistente de fluido (resistente aos anti-VEGF) são complicações da doença que, se não adequadamente tratadas, podem levar à perda visual permanente5,6.
O brolucizumabe é uma nova molécula aprovada recentemente para uso no Brasil, sendo considerada a menor unidade funcional de um anticorpo com capacidade de ligação aos receptores VEGF. Seu baixo peso molecular maximiza a quantidade de anti-VEGF em um mesmo volume a ser injetado na cavidade vítrea7. O ensaio clínico randomizado HAWK/HARRIER que avaliou a eficácia e a segurança desta droga, mostrou que cerca de 50% dos pacientes podem ser tratados com um intervalo maior entre as aplicações, quando comparados com aqueles tratados com aflibercepte, com excelente resultado funcional e com melhor resposta anatômica8. Uma recente subanálise deste estudo realizada em pacientes japoneses com VPC também mostrou resultados favoráveis ao brolucizumabe, com maior resolução de líquido sub-retiniano e sub-EPR em comparação ao aflibercepte9.
Este caso clínico ilustra o uso do brolucizumabe em um paciente portador de vasculopatia polipoidal da coroide resistente a outros agentes anti-VEGF com obtenção de melhora tanto anatômica quanto funcional.
CASO CLÍNICO
Paciente de 74 anos, sexo feminino, pseudofácica em ambos os olhos, com queixa de piora da acuidade visual do olho esquerdo (OE) iniciada em janeiro de 2021. A acuidade visual do olho direito (OD) era 20/20 e do OE era 20/60.
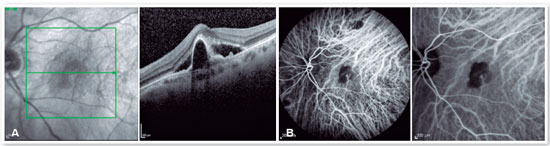
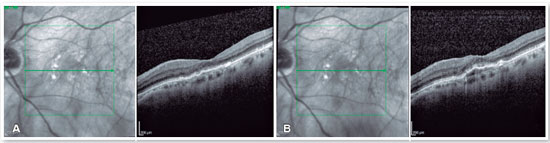
A OCT do OE revelou a presença de líquido sub-retiniano, descolamento do EPR (DEP) em forma de U invertido, material hiper-refletivo sub-retiniano e sinal da dupla camada (Figura 1A). A espessura coroideana central era reduzida (174 micra), mas notava-se a presença de paquivasos coroideanos na área subjacente ao DEP. Diante destes achados tomográficos sugestivos de vasculopatia polipoidal da coroide (VPC), foi indicada a realização de AICV, que revelou a presença de uma lesão hipercianescente nos primeiros 6 minutos de exame, correspondente à área do pólipo identificado na OCT, além de área hipocianescente circunjacente (Figura 1B). Retinografia colorida e angiofluoresceinografia complementaram a propedêutica inicial. Os exames do OD não revelaram qualquer alteração.
A paciente foi, então, submetida à dose de carregamento com três injeções intravítreas mensais de aflibercepte no OE. Após esse período, a acuidade visual piorou para 20/150 e o quadro tomográfico mostrou-se praticamente inalterado (Figura 2A). Foi indicada uma quarta injeção intravítrea de aflibercepte, novamente sem melhora tomográfica ou funcional (Figura 2B).
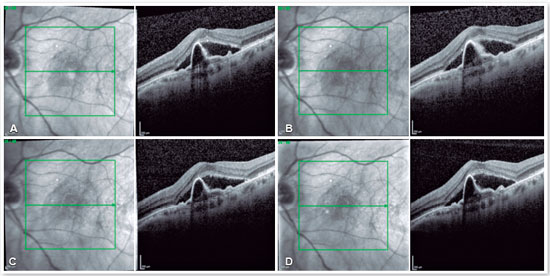
Na época, diante da impossibilidade de realização de terapia fotodinâmica (PDT) pela falta da verteporfina no país, foi indicada uma quinta injeção intravítrea de anti-VEGF, desta vez utilizando o ranibizumabe. Mais uma vez, não houve melhora anatômica ou funcional (Figura 2C). Uma sexta injeção intravítrea de anti-VEGF (aflibercepte) foi posteriormente realizada com a mesma falta de resposta anatômica e funcional (Figura 2D).
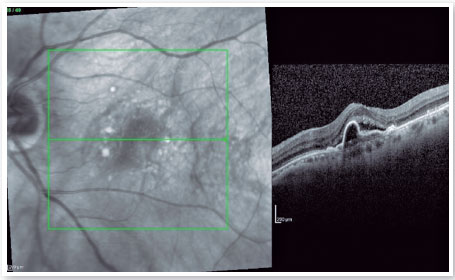
Uma sétima injeção intravítrea de anti-VEGF (ranibizumabe), desta vez associada à triancinolona intravítrea (4mg/mL), foi então realizada. Com este tratamento combinado houve uma melhora tomográfica parcial, mas sem melhora funcional (Figura 3).
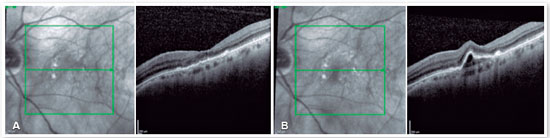
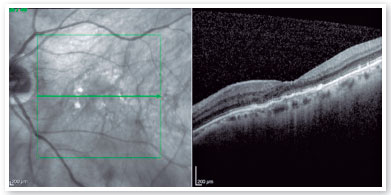
Nessa época, o brolucizumabe foi aprovado para uso no Brasil, e a droga foi, então, indicada para uso nesta paciente. Um mês após a realização da injeção intravítrea de brolucizumabe, observou-se melhora da acuidade visual para 20/100 e excelente resposta anatômica, com resolução completa do DEP e do fluido sub-retiniano (Figura 4A). A OCT realizada 8 semanas após a injeção intravítrea de brolucizumabe revelou a presença de crescimento do DEP, mas sem líquido intra ou sub-retinino associado (Figura 4B). Optou-se, então, pela realização de nova injeção intravítrea de brolucizumabe, com excelente resposta anatômica e funcional (Figura 5A). Oito semanas após a segunda dose de brolucizumabe, foi observado novo crescimento do DEP, mais uma vez sem líquido intra ou sub-retiniano associado (Figura 5B). Foi realizada, então, a 3ª injeção intravítrea de brolucizumabe. A OCT realizada 4 semanas após esta terceira dose revelou completa resolução do fluido (Figura 6). A paciente permanece em acompanhamento.
DISCUSSÃO
O presente caso apresenta características angiográficas e tomográficas sugestivas de VPC. Na angiografia com indocianina verde, a presença de lesão hipercianescente observada nos primeiros 6 minutos do exame é considerada um dos principais critérios diagnósticos de VPC5. Já a presença de descolamento do EPR em U invertido, sinal da dupla camada e descolamento do EPR multilobulado estão entre os sinais tomográficos sugestivos de VPC2,5. A característica elevação do EPR em U invertido é considerada o sinal tomográfico mais frequente em pacientes com VPC. Recente trabalho que avaliou 69 olhos com VPC observou que esta característica esteve presente em 56.4% dos casos2. Um outro achado tomográfico presente neste caso foi a espessura coroideana reduzida (175 µm) e a presença de paquivasos subjacentes à área de descolamento do EPR. Em um estudo realizado por Lee et al.3 envolvendo 320 olhos com VPC, foi encontrado uma distribuição bimodal da espessura de coroide subfoveal, com picos de 170 e 390 micra. Assim como no presente caso, no grupo com espessura de coroide reduzida foram observados paquivasos na área subjacente à lesão polipoidal.
Neste caso de VPC observamos resistência ao tratamento com várias injeções intravítreas de aflibercepte e ranibizumabe. Acredita-se que pacientes com VPC apresentam uma maior resistência ao tratamento com estas drogas do que aqueles que apresentam a forma clássica da DMRI. Kokame et al.6 avaliaram 253 olhos com DMRI exsudativa (114 olhos com VPC) e observaram que a VPC foi diagnosticada em 50% dos olhos considerados resistentes à terapia anti-VEGF (fluido sub-retiniano persistente, edema macular ou hemorragia sub-retiniana após 4 injeções intravítreas sequenciais). No presente caso, foi tentada, ainda, a associação do anti-VEGF com corticoide intravítreo, com a obtenção de melhora anatômica parcial. Embora os corticosteroides sejam uma droga off-label, seu uso pode ser excepcionalmente considerado em casos de DMRI neovascular não-responsivos10.
Já o brolucizumabe foi a única droga utilizada neste caso que proporcionou excelente resposta anatômica e funcional. Resolução rápida e completa do fluido sub-retiniano foi observada já após a primeira dose de brolucizumabe, podendo representar a inatividade, ao menos temporária, do pólipo. Embora a droga tenha sido utilizada, neste caso, a cada 8 semanas, é importante mencionar que, após este período, ainda não havia líquido intra ou sub-retiniano, tendo sido notado apenas um crescimento do DEP. A indicação de anti-VEGF em um paciente em tratamento para DMRI neovascular, em que se observa crescimento do DEP e ausência de líquido intra ou sub-retiniano é controversa, sendo que alguns autores indicam o tratamento, enquanto outros optam por conduta mais conservadora11.
Uma recente subanálise do estudo HAWK realizada em pacientes japoneses portadores de VPC mostrou que a monoterapia com brolucizumabe 6mg (a cada 8 ou 12 semanas) resultou em ganhos visuais robustos e consistentes, comparáveis aos obtidos com a monoterapia com o aflibercepte a cada 8 semanas. No entanto, os resultados anatômicos obtidos com o brolucizumabe foram nitidamente superiores em relação ao aflibercepte. Ao final de 48 semanas de tratamento, o líquido intra ou sub-retiniano esteve presente em 7,7% dos pacientes tratados com brolucizumabe e em 30% daqueles tratados com aflibercepte. Ao final de 96 semanas, o líquido intra ou sub-retiniano esteve presente em 12,8% dos pacientes tratados com brolucizumabe e em 16,7% daqueles tratados com aflibercepte. Similarmente, uma menor proporção de olhos com fluido sub-EPR foi notada nos pacientes tratados com brolucizumabe quando comparados com aqueles tratados com aflibercepte, desde a semana 4 (38,5% vs 60.0%) até a semana 96 (7,7% vs 13,3%), respectivamente. Além disso, a maior parte dos pacientes estudados (76% ao final de 48 semanas e 68% ao final de 96 semanas) recebeu esta droga a cada 12 semanas9.
A capacidade da monoterapia com brolucizumabe levar à resolução do fluido em um maior percentual de pacientes pode representar uma alternativa para pacientes com VPC que tradicionalmente teriam que ser abordados por um tratamento combinado (anti-VEGF e PDT). Desta forma, os dados da literatura e os resultados obtidos neste caso específico, mostram que o brolucizumabe é uma droga que pode ser considerada particularmente importante no tratamento da vasculopatia polipoidal da coroide, proporcionando excelentes resultados anatômicos (superiores ao aflibercepte) e funcionais, permitindo, ainda, um espaçamento maior entre as aplicações.
REFERÊNCIAS
1. Spaide RF, Jaffe GJ, Sarraf D, Freund KB, Sadda SR, Staurenghi G, et al. Consensus nomenclature for reporting neovascular age-related macular degeneration data: consensus on neovascular age-related macular degeneration nomenclature study group. Ophthalmology. 2020;127(5):616-36.
2. Kokame GT, Omizo JN, Kokame KA, Yamane ML. Differentiating exudative macular degeneration and polypoidal choroidal vasculopathy using OCT B-scan. Ophthalmol Retina. 2021;5(10): 954-961.
3. Lee WK, Baek J, Dansingani KK, Lee JH, Freund B. Choroidal morphology in eyes with polypoidal choroidal vasculopathy and normal or subnormal subfoveal choroidal thickness. Retina. 2016;36 Suppl 1:S73-S82.
4. Pereira FB, Veloso CE, Kokame GT, Nehemy MB. Characteristics of neovascular age-related macular degeneration in brazilian patients. Ophthalmologica. 2015;234(4):233-42.
5. Cheung CMG, Lai TYY, Ruamviboonsuk P, Chen SJ, Chen Y, Freund KB et al. Polypoidal choroidal vasculopathy: definition, pathogenesis, diagnosis, and management. Ophthalmology. 2018;125(5):708-24.
6. Kokame GT, DeCarlo TA, Kaneko KN, Omizo JN. Anti-vascular endothelial growth factor resistance in exudative macular degeneration and polypoidal choroidal vasculopathy. Ophthalmol Retina. 2019;3(9):744-52.
7. Nguyen QD, Das A, Do DV, Dugel PU, Gomes A, Holz FG. Brolucizumab: evolution through preclinical and clinical studies and the implications for the management of neovascular age-related macular degeneration. Ophthalmology. 2020;127(7):963-76.
8. Dugel PU, Koh A, Ogura Y, Jaffe GJ, Schmidt-Erfurth U, Brown DM, Gomes AV, Warburton J, Weichselberger A, Holz FG; HAWK and HARRIER Study Investigators. HAWK and HARRIER: Phase 3, Multicenter, Randomized, Double-Masked Trials of Brolucizumab for Neovascular Age-Related Macular Degeneration. Ophthalmology. 2020;127(1):72-84.
9. Ogura Y, Jaffe GJ, Cheung CMG, Kokame GT, Iida T, Takahashi K, et al. Efficacy and safety of brolucizumab versus aflibercept in eyes with polypoidal choroidal vasculopathy in Japanese participants of HAWK. Br J Ophthalmol. 2022;106(7):994-9.
10. Kaya C, Zandi S, Pfister IB, Gerhardt C, Garweg JG. Adding a corticosteroid or switching to another anti-VEGF in insufficiently responsive wet age-related macular degeneration. Clin Ophthalmol. 2019 Dec 5;13:2403-2409.
11. Schmidt-Erfurth U, Waldstein SM. A paradigm shift in imaging biomarkers in neovascular age-related macular degeneration. Prog Retin Eye Res. 2016 Jan;50:1-24.

Financiamento: Declaram não haver.
Conflitos de Interesse: Declaram não haver.
Recebido em:
30 de Novembro de 2022.
Aceito em:
18 de Dezembro de 2022.